厉害了!cfDNA又添新用途,或将成为新型衰老生物标志物
人类细胞中的DNA链全长近2米。看似繁杂的DNA链却规律地折叠在直径约5微米的细胞核内,并完成“编码”功能。在我们年轻的时候,DNA会规矩的待在细胞核中,但随着年龄的增长,DNA开始不再那么听话。在血液中,细胞因应激或降解释放的cfDNA仍保留了部分的组装状态,可为生物标志物研究提供信息。
近年来,表观遗传学成为研究热点。由DNA和组蛋白形成的染色质基本结构单位——核小体也是表观基因组的重要组成。在核小体中,DNA链像线轴一样缠绕着组蛋白。核小体可在不改变DNA序列的情况下影响基因表达,产生可以遗传的变化,对细胞功能产生影响。来自美国布朗大学的科学家们一直在寻找与年龄和健康相关的cfDNA差异。近日,布朗大学分子生物学教授Nicola Neretti领导的一项针对不同人群cfDNA的研究取得了重要进展,并发表在Aging Cell上。文章题为“Cell‐free DNA as a biomarker of aging”。该研究发现,健康年轻人cfDNA链上的核小体分布比较规律;在老年人,尤其是不健康的百岁老人中,核小体分布就不那么规律。此外,健康百岁老人的cfDNA核小体分布与健康年轻人更为相似!

研究发现,随着年龄的增长,两个常见转座子的cfDNA信号开始减少,表明这些转座子在不健康的百岁老人和老年人中较少被“锁定”,因此更有可能将自己“复制并粘贴”到基因组中,导致基因组的混乱。此外,在其他表观基因组特征中,健康的百岁老人与年轻个体的特征相似度较高。
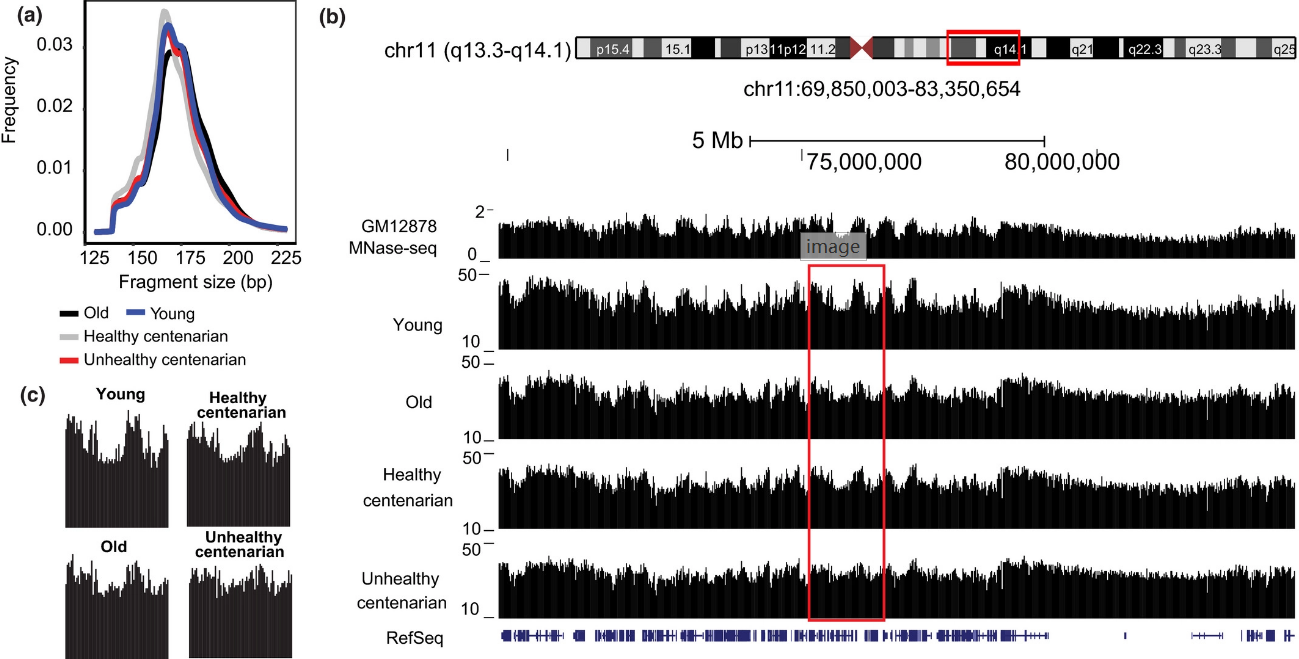
经过验证,研究团队发现,根据cfDNA推断的核小体信号与在其他模型系统观察到的细胞衰老过程中异染色质再分布是一致的。同时,研究人员还在数个基因组位置检测到cfDNA的相对缺失,包括转录起始点和终止点,L1HS反转录转座子5‘UTR等。
很多细胞器都会参与核小体间距的维持。随着年龄的增长,相关细胞器水平的降低也会对核小体间距造成不同程度的影响。核小体间距的异常改变会影响基因组不同区域的可及性,进而导致更多错误的遗传事件,包括转录翻译。该研究结果表明年龄、健康状况与不同组织中细胞DNA信号的变化有关,cfDNA可以作为一种新型衰老生物标志物,其相关差异可被用于明确生物的“准确”年龄,反映机体的健康情况。
已有研究表明,细胞一旦死亡,核小体之间的DNA就会被切割。从表观遗传的角度来看,cfDNA记录了细胞死亡前的样子。Neretti 教授表示:“有关衰老的很多分子机制是相互作用,相互关联的,但我们仍然不清楚这些相互作用的原因和后果。现在通过我们的cfDNA 检测方法,有希望了解这些表观遗传变化及衰老背后的遗传机制。”
为使分析结果更准确,该研究团队正在努力优化从血液中提取cfDNA的过程。现在,他们可以从四分之一茶匙的血样中可靠地提取所需的cfDNA量。Neretti教授认为仅需对2%~5%的基因组进行测序就足够检测整个的表观遗传变化。除了完善核小体定位分析之外,该研究团队还将研究另一种表观遗传标记——cfDNA的DNA甲基化模式,以为追溯cfDNA来源提供更多信息。该研究仅分析了12个人的cfDNA情况。研究人员表示,针对以上研究发现将进行更大规模的研究验证,并将表观基因组差异与健康状况、生活方式或饮食联系起来。研究确定不同年龄人群的cfDNA来源和特征,有助于了解哪些组织正在经历大量的细胞死亡,为了解衰老过程的表观遗传过程与衰老相关疾病提供重要信息。
一直以来,cfDNA多用于癌症等疾病的筛查与治疗监测等研究。近年来,有关cfDNA表观遗传特征的研究层出不穷,该研究的一些新发现为cfDNA在其他领域的研究应用提供了借鉴。除了衰老,或许cfDNA核小体特征在癌症等其他疾病中也有一定的影响。希望有越来越多的相关研究能够报道,不断拓展cfDNA等液体活检技术的应用范围,为精准医疗的发展进步作贡献。
参考资料:
1. Cell‐free DNA as a biomarker of aging
2. Biological Age Revealed by Epigenomic Packaging of Blood’s Cell-Free DNA
来源:测序中国


